Պարբերական համակարգը պարբերական օրենքի պատկերումն է
Պարբերական համակարգում, յուրաքանչյուր տարրի հատկացված են խիստ որոշակի համարով առանձին վանդակ՝ «բնակարաններ», որտեղ գրվում են տվյալ տարրը բնութագրող մեծությունները:
Օրինակ
\(N\) ՝արտաքին էլեկտրոնային շերտում էլեկտրոնների թիվը (վերջի երկու մեծությունների հետ կծանոթանաք հաջորդ թեմայում): էլեկտրոնների բաշխումը ատոմում ըստ էներգիական մակարդակների, \(5\) և \(2\)՝ հարաբերական ատոմային զանգվածը, \(14, 006՝ \)ատոմային համարը (կարգաթիվը), \(7\)՝ անվանումը, ազոտ` ազոտ տարրի քիմիական նշանն է,


Պարբերական համակարգը կազմված է յոթ հորիզոնական և ութ ուղղաձիգ շարքերից: Տարրերի հորիզոնական շարքը, որոնցում դիտվում է հատկությունների հետզհետե փոփոխություն` մինչև շարքի առաջին տարրի հատկությունների կրկնվելը, Մենդելեևն անվանեց պարբերություն: \(1\) -ին պարբերությունը անվանում են հատուկ, 2 -րդ և 3 -րդը՝ փոքր, 4 - 6 պարբերությունները՝ մեծ, իսկ 7 -ը՝ անավարտ: Պարբերությունները, բացառությամբ առաջինի, սկսվում են ալկալիական մետաղով և վերջանում իներտ գազով:
Ուղղաձիգ շարքերում՝ խմբերում նման հատկություններով տարրերն են իրար տակ տեղադրված: Խմբերը բաժանվում են երկու ենթախմբերի՝ գլխավոր (\(A\)) և երկրորդական (\(B\)): \(A \) -ում ընդգրկված են և՛փոքր, և՛մեծ պարբերությունների տարրեր, իսկ \(B\) -ում ՝ միայն մեծ պարբերությունների տարրեր:
Մենդելեևն ստեղծեց պարբերական համակարգ, որի կարճ ձևը բերված է ստորև.
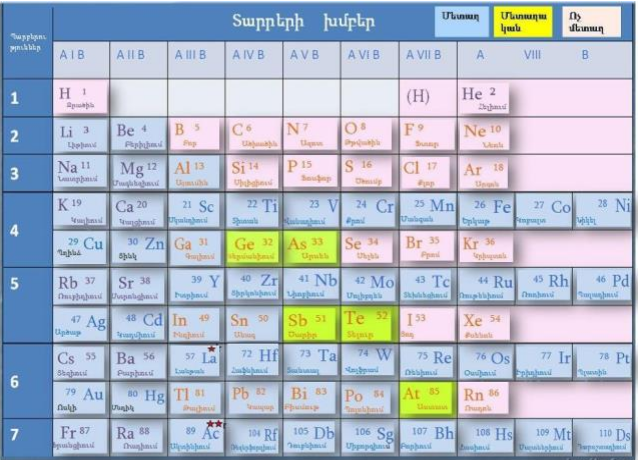
Պարբերական համակարգը բացահայտում է մի շարք օրինաչափություններ` տարրերի հատկությունների վերաբերյալ: Այդ համակարգում պարբերությունների և խմբերի համարները չափազանց կարևոր տեղեկություններ են տալիս տարրերի ատոմների կառուցվածքի, հետևաբար նաև քիմիական հատկությունների մասին:


