Բազմաթիվ նյութեր սովորական պայմաններում գտնվում են գազային ագրեգատային վիճակում:
Պինդ և հեղուկ ագրեգատային վիճակում գտնվող նյութերի մոլեկուլները, ատոմները կամ իոնները հպված են միմյանց, փոխազդում են միմյանց հետ, և հենց այդ կառուցվածքային մասնիկների սեփական չափերով է պայմանավորված նյութի ընդհանուր ծավալը: Ի տարբերություն պինդ և հեղուկ նյութերի, գազերում մոլեկուլները չեն հպվում միմյանց, նրանց միջև հեռավորությունը տասնյակ անգամներ գերազանցում է մոլեկուլների սեփական չափերը:
Գազերում միջմոլեկուլային հեռավորությունները պայմանավորված են արտաքին պայմաններով՝ ջերմաստիճան և ճնշում: Այդ պատճառով գազերն ունեն մի շարք ըհդհանուր ֆիզիկական հատկություններ: Օրինակ՝ բոլոր գազերի սեղմելիության հատկությունը նույնն է (Բոյլ-Մարիոտի օրենք), կամ՝ բոլոր գազերն ունեն նույն ջերմային ընդարձակման գործակից (Գեյ-Լյուսակի օրենք) և այլն:

1. գազ 2. հեղուկ 3. պինդ
Օրինակ՝ գոլորշի (1) և հեղուկ (2) վիճակներում գտնվող ջրի մոլեկուլների միջև հեռավորությունները խիստ տարբեր են. գոլորշին հեշտությամբ սեղմվում է, իսկ հեղուկ ջուրը՝ ոչ:
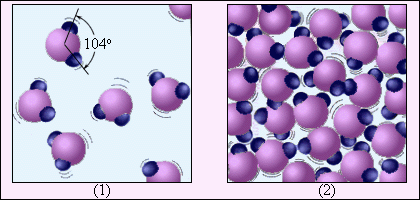
Գազի ծավալը որոշվում է ոչ թե գազի մոլեկուլների սեփական չափսերով, այլ միջմոլեկուլային հեռավորություններով, ինչն էլ իր հերթին պայմանավորված է արտաքին պայմաններով՝ ճնշումով և ջերմաստիճանով:
Բազմաթիվ դիտարկումներից հետո իտալացի անվանի գիտնական Ամադեո Ավոգադրոն \(1811\) թվին առաջարկեց մի վարկած, որն այնուհետև ապացուցվեց և ձևակերպվեց որպես Ավոգադրոյի օրենք:
Տարբեր գազերի հավասար ծավալներում արտաքին միատեսակ պայմաններում (ճնշում, ջերմաստիճան) պարունակվում են հավասար թվով մոլեկուլներ:
Հայտնի է, որ մոլեկուլային կառուցվածք ունեցող յուրաքանչյուր նյութի մեկ մոլը պարունակում է թվով մոլեկուլներ: Ավոգադրոյի օրենքից բխում է, որ մեկ մոլ քանակով ցանկացած գազի զբաղեցրած ծավալը պետք է լինի հաստատուն: Նորմալ պայմաններում (ն.պ.) (, \(101,3\) կՊա ճնշում) այն կազմում է \(22,4 \) լիտր և կոչվում է գազի մոլային ծավալ.
Սովորական պայմաններում գազեր են ոչ մետաղային տարրերի առաջացրած որոշ պարզ նյութեր՝ ջրածին, թթվածին, օզոն, ազոտ, քլոր, ֆտոր, որոշ ոչ մետաղային տարրերի ջրածնային միացություններ՝ մեթան, ամոնիակ, ացետիլեն, քլորաջրածին, ֆտորաջրածին, բրոմաջրածին, յոդաջրածին, սիլան և այլն, որոշ ոչ մետաղների օքսիդներ՝ ածխածնի, ազոտի և քլորի որոշ
օքսիդները, բոլոր իներտ գազերը՝ հելիում, նեոն, արգոն, կրիպտոն, քսենոն և այլն:




և այլն:
Հեղուկ և պինդ նյութերի մոլային ծավալները պայմանավորված են իրենց խտություններով և միմյանցից խիստ տարբեր են:
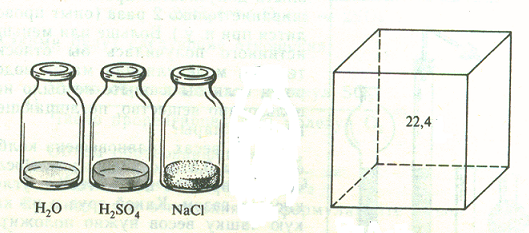
Որոշակի մոլ քանակով գազի ծավալը կարող ենք հաշվել հետևյալ բանաձևի միջոցով՝
Օրինակ` \(3\) մոլ ջրածնի ծավալը նորմալ պայմաններում հավասար է.


