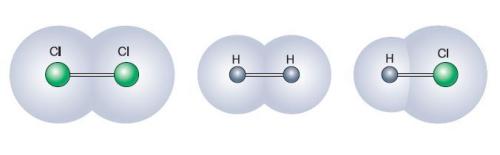
Ոչ բևեռային և բևեռային կովալենտային կապեր
Եթե կովալենտային կապն առաջանում է նույն տարրի երկու ատոմների միջև, ապա այն կոչվում է ոչ բևեռային կովալենտային կապ:
Օրինակ ջրածնի մոլեկուլում կովալենտային կապն առաջանում է \(s-\) ատոմային օրբիտալների \(s-s\) փոխծածկմամբ:
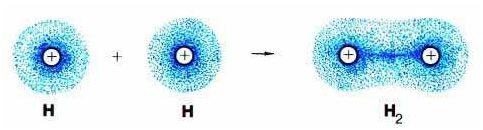
Կամ՝
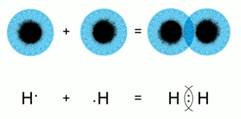
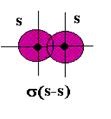
Քլորի, ֆտորի մոլեկուլներում կովալենտային կապն առաջանում է \(p-\) ատոմային օրբիտալների \(p-p\) փոխծածկմամբ:
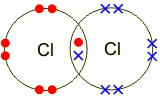
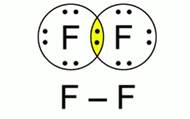
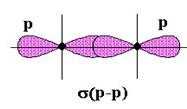
Ընդհանրացված էլեկտրոնային զույգը կամ օրբիտալների փոխծածկի տիրույթը գտնվում է միջուկներից հավասար հեռավորության վրա, բացասական լիցքը երկու միջուկների միջև բաշխվում է համաչափորեն, այսինքն՝ լիցքերի բևեռացում տեղի չի ունենում:
Ոչ բևեռային կովալենտային կապ առկա է, հիմնականում, պարզ նյութերի մոլեկուլներում, սակայն, այդպիսի կապ կարող է լինել նաև բարդ նյութերի մոլեկուլներում:
Օրինակ՝ ջրածնի պերօքսիդի՝ , մոլեկուլում թթվածնի ատոմների միջև առկա է ոչ բևեռային կովալենտային կապ:
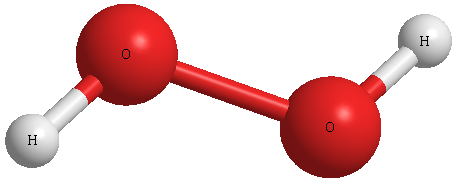
Նույն՝ -ի մոլեկուլում \(H-O\) կապերը բևեռային են:
\(H-Cl\), \(H-Br\) մոլեկուլներում կապն առաջանում է \(s-\) և \(p-\) ատոմային օրբիտալների \(s-p\) փոխծածկմամբ:


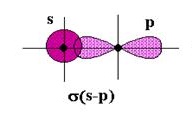
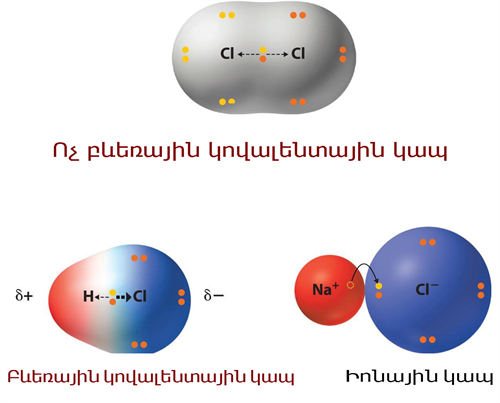
Այս դեպքերում ընդհանուր էլեկտրոնային զույգը կամ օրբիտալների փոխծածկի տիրույթը խտանում, բևեռանում է դեպի առավել էլեկտրաբացասական տարրի ատոմը, մոլեկուլի այդ մասը ձեռք է բերում մասնակի բացասական, իսկ մյուս մասը՝ մասնակի դրական լիցք: Այդպիսի կապը կոչվում է բևեռային կովալենտային կապ:
Օրինակ քլորաջրածնի մոլեկուլում կապը բևեռային կովալենտային է:
Որքան մեծ լինի տարրերի էլեկտրաբացասականությունների տարբերությունը, այնքան ավելի բևեռացած կլինի կովալենտային կապը:
Եթե այդ տարբերությունը շաը մեծ է (հիմնականում մետաղ-ոչ մետաղ), ապա կովալենտային կապը «վերածվում է» իոնականի, այսինքն ընդհանրացված էլեկտրոնային զույգն անցնում է տարրերից մեկին:
Ոչ բևեռային, բևեռային կովալենտային և իոնային կապերի համեմատումը կարելի է տեսնել հետևյալ նկարում.
Սիգմա և պի կովալենտային կապեր.
Քննարկված բոլոր դեպքերում կովալենտային կապն առաջանում էր ատոմային օրբիտալների փոխծածկմամբ՝ ատոմների միջուկները միացնող առանցքի ուղղությամբ և կոչվում է սիգմա` կապ:
Ուշադրություն
Բոլոր միակի կապերը սիգմա՝ , կապեր են:
Նույն ատոմների միջև երկրորդ, երրորդ կապերի առաջացումը կատարվում է \(p\)- ատոմային օրբիտալների կողմնային, կրկնակի փոխծածկմամբ՝ միջուկները միացնող առանցքի երկու կողմերում և կոչվում է պի՝ կապ: Օրինակ էթենի մոլեկուլում ածխածնի ատոմների միջև առաջին կապը կապ է, իսկ երկրորդը՝ :
Վերջին դեպքում ատոմային օրբիտալների փոխծածկը կատարվում է ավելի փոքր չափով, ինչի պատճառով կապի էներգիան փոքր է կապի համեմատությամբ:
Ուշադրություն
Բազմակի կապերից միայն մեկը կարող է լինել սիգմա՝ կապ:
Կան բազմաթիվ կապ պարունակող նյութեր, օրինակներ՝

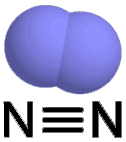
ածխածնի (IV) օքսիդ ազոտ
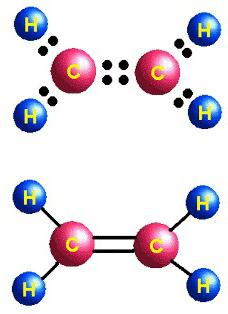
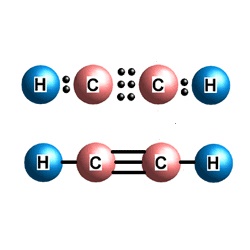
էթիլեն (էթեն) ացետիլեն (էթին)
Աղբյուրները
Ա․ ԽԱՉԱՏՐՅԱՆ, Լ․ ՍԱՀԱԿՅԱՆ
Քիմիա-10, Երևան-2010