Ֆոսֆորի օքսիդ: Ֆոսֆորական թթու
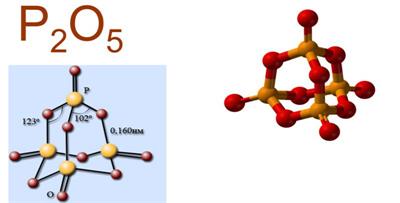
Ֆոսֆորի\((V)\) օքսիդը ֆոսֆորի առավել կայուն օքսիդն է սովորական պայմաններում։ Այն սպիտակ, ձյունանման պինդ նյութ է, որի մոլեկուլն ունի բաղադրությունը (-ը նրա պարզագույն բանաձևն է):
Ֆոսֆորի \((V)\) օքսիդն օժտված է թթվային օքսիդներին բնորոշ հատկություններով: Ոստի այն կարող է փոխազդել հիմնային օքսիդների և հիմքերի հետ:
Օրինակ՝
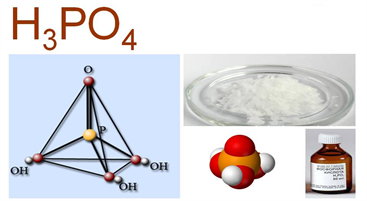
Ֆոսֆորի\((V)\) օքսիդի և ջրի փոխազդեցությունից առաջանում են ֆոսֆորական թթուներ: Գոյություն ունեն ֆոսֆորի \((V)\) օքսիդին համապատասխանող մի քանի թթու, որոնք միմյանցից տարբերվում են օքսիդի մոլեկուլին միացած ջրի մոլեկուլների քանակով: Եթե ֆոսֆորական անհիդրիդը լուծե՛ք սառը ջրում, ապա կստացվի մետաֆոսֆորական թթու՝ , որը թունավոր նյութ է.
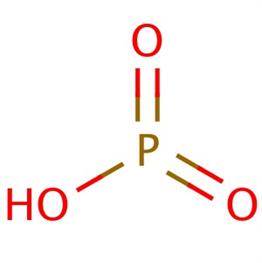
Տաք ջրում ֆոսֆորի\((V)\) օքսիդը լուծելիս ստացվում է օրթոֆոսֆորական թթու կամ պարզապես ֆոսֆորական թթու՝
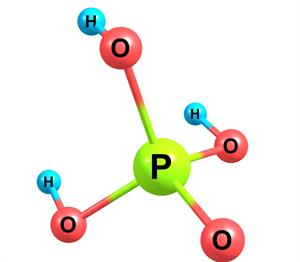
Ֆոսֆորական թթվի մոլեկուլի մոդելը
Ֆոսֆորական թթուն եռահիմն թթու է, ջրային լուծույթում ենթարկվում է աստիճանական դիսոցման.
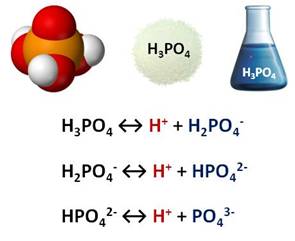
Աստիճանական դիսոցման հետևանքով ֆոսֆորական թթուն երեք տեսակի աղ է առաջացնում, չեզոք աղեր՝ ֆոսֆատներ (օրինակ՝ ), թթու աղեր՝ երկհիդրոֆոսֆատներ (օրինակ՝ ) և հիդրոֆոսֆատներ (օրինակ՝ )
Ֆոսֆորական թթուն փոխազդելով մետաղների, մետաղների օքսիդների, հիմքերի և աղերի հետ առաջացնում է այդ թթվին համապատասխանող աղեր՝ ֆոսֆատներ:
Օրինակ՝
Ֆոսֆորական թթվի աղերը լայնորեն օգտագործվում եմ որպես պարարտանյութեր:

1. Հասարակ սուպերֆոսֆատը ստանում են ըստ հետևյալ ռեակցիայի`
2. Կրկնակի սուպերֆոսֆատը ստանում են ըստ հետևյալ ռեակցիայի`
3. Պրեցիպիտատը ստանում են ըստ հետևյալ ռեակցիաների`
Աղբյուրները
Լ.Ա.Սահակյան և ուրիշներ, քիմիա 9, Երևան 2015